Artikel ini akan membahas rumus kimia lainnya yaitu rumus empiris dan rumus molekul. Bagaimana cara mengetahui rumus molekul senyawa ini? Tenang, sebelum menuju lebih dalam terkait kedua rumus ini ada baiknya kita tetap berkenalan dulu. Apa sih rumus molekul itu? Apa itu rumus empiris? Makanya, jangan sampai kalian tidak tahu mengenai dasarnya ya.
Pengertian Rumus Empiris dan Rumus Molekul
Rumus molekul adalah kelipatan-kelipatan dari rumus empiris. Rumus molekul merupakan rumus sebenarnya dari suatu senyawa. Rumus ini digolongkan menjadi dua, yaitu rumus molekul unsur dan rumus molekul senyawa.
Rumus molekul dari suatu senyawa menunjukkan jumlah atom sebenarnya dari masing-masing unsur dalam satu molekul senyawa tersebut. Jadi, rumus molekul dari karbon dioksida adalah CO2; setiap molekul karbon dioksida terdiri dari 1 atom karbon dan 2 atom oksigen.
Rumus empiris dari suatu senyawa menunjukkan jumlah atom relatif dari masing-masing unsur dalam molekul senyawa tersebut dengan rasio (perbandingan) bilangan bulat paling sederhana.
Sebagai contoh, rumus empiris dari asam askorbat adalah C3H4O3, di mana perbandingan jumlah atom karbon, hidrogen, dan oksigen adalah 3 : 4 : 3. Untuk lebih mengerti hal ini kalian bisa lihat kumpulan rumus asam dan basa yang sudah gue buatkan.
Data yang diperlukan untuk menentukan rumus molekul
- Menentukan dahulu rumus empiris merupakan rumus yang paling sederhana dari suatu molekul yang menunjukkan perbandingan atom-atom penyusun molekul. Untuk menentukan rumus empiris diperlukan komposisi massa unsur unsur penyusun senyawa kemudian kita bandingkan mol masing masing unsur tersebut.
- Massa molekul relatif merupakan jumlah total dari massa atom relatif unsur-unsur penyusunnya dalam suatu senyawa atau molekul, untuk mengetahui rumus molekul dari senyawa yang kita cari berapa kali kelipatan dari rumus empiris.
Bagaimana cara menentukan rumus empiris?
- Tentukan jumlah mol masing-masing unsur dalam senyawa, dan
- Tentukan perbandingan jumlah mol terkecil dari atom unsurnya.
Rumus Empiris dan Kadar Unsur dalam Senyawa
Kadar unsur dalam senyawa umumnya dinyatakan dalam persen massa unsur tersebut terhadap massa senyawa. Kadar unsur juga dapat dinyatakan sebagai massa unsur dalam 1 mol senyawa dibagi dengan massa molar senyawa tersebut lalu dikali dengan 100 persen. Massa unsur dalam 1 mol senyawa sama dengan jumlah mol unsur (n) dalam 1 mol senyawa dikalikan dengan massa molar unsur.
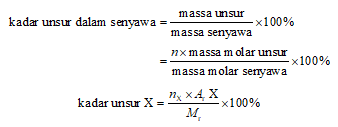
Sampai disini, sudah paham belum? Semoga kalian yang membaca artikel ini bisa paham dengan apa yang saya jelaskan disini ya. Kalian juga bisa lihat beberapa aplikasi rumus kimia yang bisa kalian gunakan gratis. Kalau ada yang belum paham terkait rumus empiris dan rumus molekul ini, silahkan ditanyakan pada kolom komentar ya.